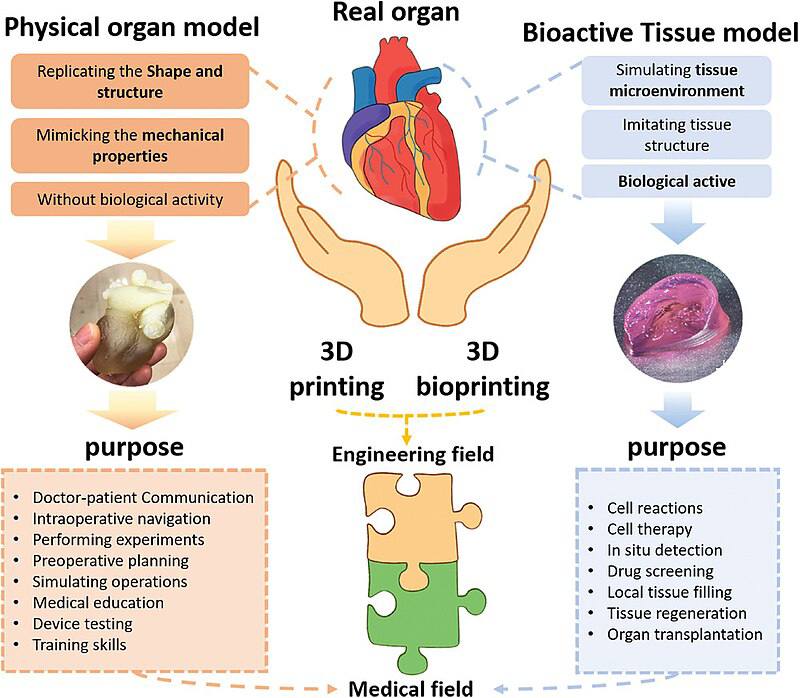
اندام های انسان ساختارهای بسیار پیچیده ای هستند که از سازماندهی ترکیبی و عملکردی انواع بافت های متعدد تشکیل شده اند. سلول های این اندام ها بسیار تخصصی هستند و برای انجام عملکردهای متمایز با هم گروه می شوند.
اختلال عملکرد یا نارسایی اندام به دلیل آسیب تروماتیک و بیماری به شدت در حال افزایش است.
اغلب، درمانهای بالینی به دلیل کمبود اهداکنندگان در دسترس و رد ایمنی بافت اهدایی محدود میشوند.در جستجوی جایگزینهایی برای استراتژیهای درمان مرسوم برای ترمیم یا جایگزینی بافتها و اندامهای انسانی از دست رفته یا ناکارآمد، رویکردهای مهندسی بافت بهعنوان یک راهحل امیدوارکننده بررسی شده اند.
هدف مهندسان زیستی ، نوآوری در استراتژیهای بازسازی بافت برای تسهیل ترمیم اندامها و همچنین تشکیل یک ابزار ترانوستیک برای انجام غربالگری دارو، با بازسازی اجزای خاص اندامهای انسان در آزمایشگاه است.
در سه دهه گذشته، پرینت زیستی سه بعدی به طور گسترده ای توسعه یافته است تا به طور مستقیم یا غیرمستقیم داربست های سلولی سه بعدی یا ایمپلنت های پزشکی را برای رشته پزشکی احیا کننده بسازد. این کنترل مکانی و زمانی بسیار دقیقی را بر روی قرار دادن سلولها، پروتئینها، DNA، داروها، فاکتورهای رشد و سایر مواد فعال زیستی برای هدایت بهتر تشکیل بافت برای درمان خاص بیمار ارائه میدهد.
یک نیاز ضروری برای بازتولید معماری پیچیده و ناهمگون بافتها یا اندامهای عملکردی، درک جامع از ترکیب و سازماندهی اجزای آنهاست.بنابراین، فناوری تصویربرداری پزشکی ابزاری ضروری برای ارائه اطلاعات در مورد ساختار و عملکرد سهبعدی است. در سطوح سلولی، بافتی، اندام و ارگانیسم، به طراحی یک ساختار خاص برای بیمار کمک می کند.معمولاً تصویربرداری غیرتهاجمی از جمله توموگرافی کامپیوتری (CT) و تصویربرداری رزونانس مغناطیسی (MRI) و همچنین ابزارهای طراحی به کمک کامپیوتر (CAD) و ساخت به کمک کامپیوتر (CAM) و مدل سازی ریاضی برای جمع آوری و دیجیتالی کردن اطلاعات پیچیده توموگرافی و معماری برای بافت ها استفاده می شود.

مدل بافت یا اندام تصویر سه بعدی به برش های افقی دو بعدی تقسیم می شود که برای رسوب لایه به لایه به یک سیستم چاپگر زیستی سه بعدی وارد می شوند. با در نظر گرفتن تکنیک های چاپ زیستی سه بعدی موجود، انواع سلول ها (متمایز یا تمایز نیافته)، مواد زیستی (مصنوعی یا طبیعی)، و عوامل بیوشیمیایی حمایت کننده انتخاب می شوند و پیکربندی این اجزای چاپ باعث ایجاد بافت ها و اندام های سه بعدی می شود. این تکنیک یکپارچه (تصویربرداری-طراحی-ساخت) می تواند ساختارهای پیچیده تری در سطح اندام سه بعدی را بازآفرینی کند و نشانه های مکانیکی و بیوشیمیایی را که عناصر حیاتی کل معماری اندام هستند، در خود جای دهد.
علاوه بر این، این تکنیک ظرفیت ایجاد یک ریزمحیط سه بعدی بافت یا اندام خاص را با تقلید از ساختارهای سه بعدی طبیعی، خواص مکانیکی و ریزمحیط های بیوشیمیایی دارد.به این ترتیب، چاپ زیستی سه بعدی برای بازسازی اندام شامل استراتژیهای اضافی برای چاپ سلولهای زنده چندگانه، از جمله یکپارچهسازی عروق و شبکه عصبی و در نهایت توسعه عملکردهای خاص آنالوگهای چاپ زیستی سه بعدی اندام است.
پرینت زیستی سه بعدی سه مفهوم اساسی را با پرینت دو بعدی معمولی به اشتراک می گذارد – چاپگر رومیزی (چاپگر سه بعدی)، فایل چاپی (فایل مدل سه بعدی)، جوهر (جوهر متشکل از مواد زیستی، اجزای زیست فعال و سلول ها) و کاغذ (سکوی چاپ). بر خلاف پرینت دوبعدی، پرینت زیستی سه بعدی فرآیندی جامع است که به ملاحظات طراحی مختلفی نیاز دارد، از جمله تصویربرداری، مدلسازی، انتخاب چاپگر، انتخاب بیووانک، شرایط کشت و توسعه ساختار سه بعدی. به طور کلی، فعالیت های تولیدی را می توان به سه مرحله تقسیم کرد: پیش از چاپ زیستی (مدل سازی)، چاپ زیستی و پس از چاپ زیستی.
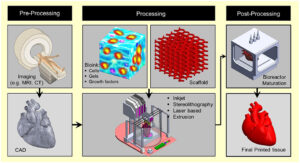
پیش چاپ زیستی، که به عنوان مدلسازی نیز شناخته میشود، عمدتاً شامل تصویربرداری سه بعدی، طراحی دیجیتالی سه بعدی و انتخاب بیواینک/مواد زیستی بر اساس نوع مدل چاپ زیستی سه بعدی است.
پس ساختار سه بعدی با طراحی خاص بیمار در فرآیند مدلسازی رسوب لایه به لایه در مرحله چاپ زیستی چاپ میشود. با توجه به طراحی برنامه چاپگرهای مختلف، فایلهای طراحی سه بعدی را میتوان مستقیماً در چاپگر بارگذاری کرد، یا ابتدا باید قبل از وارد شدن به چاپگر، از یک برنامه برش برای اصلاح بیشتر عبور کرد. برنامه برش می تواند جسم جامد را به یک پشته از مقاطع نازک و محوری تجزیه کند. هر مقطع 2 بعدی مربوطه با ادغام الگوهای پرکننده مختلف، همانطور که برنامه ریزی شده است، تکثیر می شود. در این مرحله، چاپگر فایل stl را میخواند و لایههای متوالی مایع، پودر یا چند ماده دیگر را برای ساخت مدل سهبعدی از مجموعهای از مقاطع دوبعدی میگذارد. چندین تکنیک پرینت سه بعدی قادر به استفاده از چندین نازل (چندین ماده)، زوایای قابل تنظیم و حتی چندین ترکیب چاپ هستند.
چاپ سه بعدی برای کاربردهای مهندسی بافت را می توان به دو شکل تقسیم کرد، با و بدون سلول های زنده گنجانیده شده که مستقیماً در سازه ها چاپ می شوند. تکنیکهای چاپ زیستی سلولی میتوانند مستقیماً جوهرهای زیستی را با سلولهای زنده ذخیره کنند تا یک ساختار زنده سه بعدی تشکیل دهند. بر اساس استراتژی های کاری، آنها را می توان در درجه اول به سه دسته تقسیم کرد، چاپ زیستی مبتنی بر قطره، بر اساس اکستروژن و چاپ زیستی به کمک لیزر. در مقایسه، تکنیکهای چاپ زیستی بدون سلول، انتخابهای گستردهتری برای کاربردهای بازسازی بافت فراهم میکنند.بدون در نظر گرفتن قابلیت زنده ماندن سلول یا اجزای زیست فعال، چندین تکنیک پرینت سه بعدی با دماهای بالاتر، مواد شیمیایی و سایر محیط های خشن را می توان برای ساخت ایمپلنت ها مورد استفاده قرار داد.
در نهایت، دوره ی پس از چاپ زیستی، که شامل توسعه ساختارهای بیومیمتیک، پشتیبانی مکانیکی و عملکرد بیولوژیکی است، یک گام اساسی برای توسعه بافت ها/ اندام های بالغ برای کاربردهای زنده است. از جمله، به طور بالقوه برای ایجاد کشش مکانیکی / مقاومت بالاتر، ساختارهای دقیق تر، ساختارهای پیچیده تر مورد نیاز است.
اولین اندام چاپ شده زیستی: در سال 2019، محققان با موفقیت یک قلب کوچک انسان را با سلول ها، رگ های خونی و سایر اجزای زیستی چاپ کردند.
دانشمندان به قلبی به اندازه خرگوش با شبکهای از رگهای خونی که میتوانستند مانند رگهای خونی طبیعی منقبض شوند ، دست یافتند.قلب چاپی ساختار و عملکرد آناتومیک درستی در مقایسه با قلب های واقعی داشت.این پیشرفت نشان دهنده امکان واقعی چاپ اندام های انسان با عملکرد کامل بود
انواع جوهر زیستی: جوهرهای زیستی می توانند شامل سلول های بنیادی، هیدروژل و اجزای ماتریکس خارج سلولی برای تقلید از بافت واقعی باشند.
درمان شخصی : از آنجایی که بافتهای چاپشده زیستی را میتوان از سلولهای خود بیمار ساخت، خطر رد عضو بسیار کاهش مییابد.
چالش ها : در حالی که بافتهای ساده مانند پوست یا غضروف به صورت زیستی چاپ شدهاند، ایجاد اندامهای پیچیده مانند کلیهها یا کبد به دلیل ساختار پیچیدهشان همچنان یک چالش است.
تأثیر اخلاقی: چاپ زیستی این پتانسیل را دارد که با ایجاد بافتهای انسانمانند برای آزمایش دارو، اتکا به آزمایشهای حیوانی را کاهش دهد.
References :
https://pmc.ncbi.nlm.nih.gov/articles/PMC5313259/#:~:text=Here%2C%20a%20universal%20cell%20seeding,or%20structural%20support%20during%20healing.
https://www.sciencedirect.com/science/article/pii/S2095809924003163
https://communities.springernature.com/posts/the-art-of-3-d-bioprinting-for-organ-regeneration
https://www.frontiersin.org/journals/mechanical-engineering/articles/10.3389/fmech.2020.589171/full